group-telegram.com/survmed03/2346
Last Update:
Гипероксия и черепно-мозговая травма в остром периоде
Romero‑Garcia at al. показали, что существует связь между поддержанием PaO2 в артериальной крови и неврологическими исходами черепно-мозговой травмы (ЧМТ). Мозг весьма уязвим к чрезмерному окислительному стрессу и активным формам кислорода. Авторы показали, что высокое содержание PaO2 (гипероксемия) была связана с плохими неврологическими исходами и смертностью. До сих пор некоторые интенсивисты стараются вести пациентов с ЧМТ в гипероксии, опасаясь гиперкапнии и сопутствующего отека мозга. Необходимо скорректировать стратегию кислородной поддержки в этой популяции. Физиологические эффекты O2, гипероксии и гипоксии на мозговой кровоток и метаболизм известны.
При окислительном стрессе активные виды кислорода ухудшают исход. Это объясняет связь с гипероксией. Но давайте также вспомним некоторые фундаментальные аспекты физиологии. Активные формы кислорода являются обычным продуктом аэробного метаболизма и образуются внутри клетки, а именно в митохондриях. Их чрезмерное производство наблюдается в том числе, когда концентрация O2 резко меняется (синдром ишемии-реперфузии) за счет производства супероксидных анионов в фазе реперфузии.
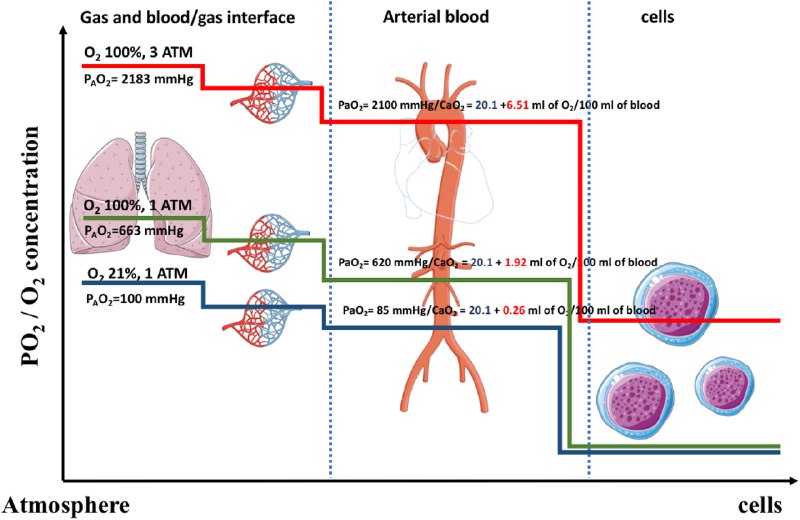
Однако и эта гипотеза слишком упрощена. Гипероксемия - это супернормальное количество О2 в крови (при условии что норма - это концентрация у здорового человека на уровне моря). В клинической практике это оценивают по PaO2 (парциальное давление растворённого О2) или общему содержанию О2 (в том числе внутри гемоглобина). Гипероксия наблюдается, когда супернормальные концентрации O2 попадают внутрь клеток. В нормобарических и нормотермических условиях абсолютное количество растворённого транспортируемого О2 очень низкое. При этом коэффициент растворимости О2 в крови тоже низкий. Для обеспечения доставки О2 нам необходима система-носитель - гемоглобин. Однако только растворимые формы О2 могут проникать в ткани.
На уровне тканей гемоглобин "выгружает" молекулы О2 по мере того как PaO2 снижается в соответствии с локальными потребностями тканей (эффект Бора). Следовательно в стандартных условиях количество дополнительного О2, введенного пациенту (FiO2) и время, затраченное на оксигенотерапию (единица токсичности кислорода, используется водолазами) являются основными переменными. Непосредственно подвергаются воздействию О2 клетки эпителия дыхательных путей. Другие ткани защищены эффектом Бора и реакциями микроциркуляции. Недавнее исследование потребления О2 при глубоком гипотермическом сердечно-легочном шунтировании во время эндартеректомии показало, что несмотря на возрастание PaO2 до 500 мм.рт.ст. и выше (в ответ на охлаждение до 18 градусов) вено-артериальная разница О2 снизилась (в соответствии с потребностями метаболизма при гипотермии). Клетки использовали только то количество О2, которое им требовалось. То есть гипероксемия - не то же самое что гипероксия. Еще одно пилотное исследование сравнило уровень активных форм кислорода при FiO2 40% и 70% у пациентов с ЧМТ на ИВЛ. Уровень совпал в целом у двух групп, что говорит о том, что связь между гипероксемией и окислительным стрессом не так очевидна.
Влияние гипероксемии на мозговой кровоток широко изучено у животных и человека. В нормобарических условиях дыхание чистым кислородом незначительно снижает мозговой кровоток при постоянном уровне PaO2 и PaCO2 в артериях. В том числе на мозговой кровоток влияет pH, режим ИВЛ, наличие спонтанного дыхания и механизмы ауторегуляции. Реакция на PaO2 и PaCO2 может притупляться и обостряться после ЧМТ. Гипероксемическая вазоконстрикция является защитным механизмом, ограничивающим доступ О2 к клеткам. Эта местная микроциркуляторная реакция на повышение концентрации О2 в артериолах. Хотя ее механизм еще не изучен, маловероятно, что свою роль тут играют простагландины. Роль лейкотриенов представляется более убедительной. Воздействие PaO2 на метаболизм мозга является физиологическим обоснованием эффективности гипербарической оксигенации (ГБО) после черепно-мозговой травмы, инсульта и при постаноксичечкой энцефалопатии.
BY Ночная охота
Share with your friend now:
group-telegram.com/survmed03/2346
